三氯氧钒
化合物
三氯氧釩,化學式為VOCl3的無機物。這種物質可通過蒸餾的方法得到,在空氣中十分容易水解,是一種強氧化劑。在有機合成中充當反應試劑。[1]
| 三氯氧釩 | |
|---|---|

| |
| |
| IUPAC名 三氯氧釩 | |
| 别名 | 釩酰氯 |
| 识别 | |
| CAS号 | 7727-18-6 |
| PubChem | 24410 |
| RTECS | YW2975000 |
| 性质 | |
| 化学式 | VOCl3 |
| 摩尔质量 | 173.30 g·mol⁻¹ |
| 外观 | 棕黃色液體 |
| 密度 | 1.826 g/cm3,液態 |
| 熔点 | -76.5 °C(197 K) |
| 沸点 | 126.7 °C(400 K) |
| 溶解性(水) | 分解 |
| 溶解性(其他溶劑) | 含氯溶劑 |
| 蒸氣壓 | 8.1 Pa(20 °C) |
| 结构 | |
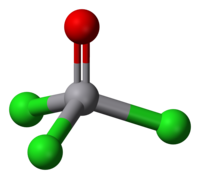
| 分子构型 | 四面體 |
| 危险性 | |
| 欧盟编号 | 沒列出 |
| 主要危害 | 有毒,水解生成HCl |
| NFPA 704 | |
| 致死量或浓度: | |
LD50(中位剂量)
|
140 mg/kg(老鼠,口服) |
| 相关物质 | |
| 相关釩化合物 | 五氧化二釩 四氯化釩 三氟氧釩 |
| 相关化学品 | 三氯氧磷 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
性質 编辑
三氯氧釩的釩呈正五價,並有反磁性。其分子構形為正四面體,其中O-V-Cl鍵鍵角為111°,Cl-V-Cl鍵鍵角為108°,V-O鍵和V-Cl鍵健長分別為157和214pm。三氯氧釩在水中反應劇烈,靜置時會產生氯氣。其可溶於非極性溶劑,如苯,二氯甲烷,己烷。在某種程度上,三氯氧釩和三氯氧磷化學性質相似。一個不同點是,三氯氧釩是強氧化劑,而磷化物不是。[2]
製備 编辑
VOCl3可由V2O5與氯氣反應製得,反應過程中,環境溫度約保持在600°C:[3]
- 3 Cl2 + V2O5 → 2 VOCl3 + 1.5 O2
當V2O5和碳混合,環境溫度在200-400 °C時,碳會充當脫氧劑,就像碳在克羅爾法中將TiO2轉化為TiCl4的作用一樣。
三氧化二釩也可用作反應前體物:
- 3 Cl2 + V2O3 → 2 VOCl3 + 0.5 O2
- V2O5 + 3 SOCl2 → 2 VOCl3 + 3 SO2
相關反應 编辑
水解和醇解 编辑
三氯氧釩在水中會迅速水解為五氧化二釩和鹽酸。在化學框模板的最上面一幅圖中,可見到在燒杯壁有橙色的V2O5生成。該過程中間會有VO2Cl生成:
- 2 VOCl3 + 3 H2O → V2O5 + 6 HCl
VOCl3可與醇類反應,生成醇鹽,特別是在質子接受體(如Et3N)前面:
互換成其他V-O-Cl化合物 编辑
VOCl3也可用於合成VOCl2:
- V2O5 + 3 VCl3 + VOCl3 → 6 VOCl2
- VOCl3 + Cl2O → VO2Cl + 2 Cl2
大於180°C時,VO2Cl分解為V2O5和VOCl3。同樣,VOCl2也可分解為VOCl3和VOCl。
加合物 编辑
VOCl3是一種強路易斯酸,其趨向於與乙腈、胺等各種鹼基形成加合物。在形成的加合物中,釩會由原先的V4幾何四面體變為V6八面體:
- VOCl3 + 2 H2NEt → VOCl3(H2NEt)2
VOCl3用於烯烴聚合 编辑
VOCl3在製備乙丙橡胶(實三元乙丙橡胶,EPDM)的反應中可用作催化劑或預催化劑。
參考來源 编辑
- ^ M. O'Brien, B. Vanasse. Encyclopedia of Reagents for Organic Synthesis. 2001.
- ^ A. Earnshaw, N. Greenwood. The Chemistry of the Elements - Second Edition. 1997: 513–514.
- ^ A. Holleman, E. Wiberg. Inorganic Chemistry. 2001.
- ^ S. Tyree. Inorganic Syntheses Volume IX. 1967: 80.
- ^ H. Oppermann, "Gleichgewichte mit VOCl3, VO2Cl, VOCl2" Zeitschrift für Anorganische und Allgemeine Chemie, vol. 331. 113-126 (1967)
