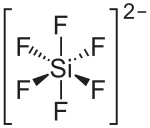
氟硅酸钾
化合物
氟硅酸钾(Potassium fluorosilicate),别名硅氟化钾,化学式K2SiF6。分子量220.26。
| 氟硅酸钾 | ||
|---|---|---|
|
| ||
| 别名 | 六氟硅酸钾 | |
| 识别 | ||
| CAS号 | 16871-90-2 | |
| PubChem | 61851 | |
| SMILES |
| |
| EINECS | 240-896-2 | |
| 性质 | ||
| 化学式 | K2SiF6 | |
| 摩尔质量 | 220.28[1] g·mol⁻¹ | |
| 外观 | 白色固体[2] | |
| 密度 | 2.27 g/cm−3[1] 2.719 g/cm−3 [3] | |
| 溶解性(水) | 1.77 g/L 当 20℃[2] | |
| 溶解性 | 不溶于液氨[4] 和酒精[5] | |
| 危险性 | ||
GHS危险性符号
| ||
| GHS提示词 | Danger | |
| H-术语 | H301, H311, H331 | |
| P-术语 | P261, P264, P270, P271, P280, P301+310, P302+352, P304+340, P311, P312, P321, P322, P330, P361 | |
| 致死量或浓度: | ||
LD50(中位剂量)
|
156 mg/kg[2] | |
| 相关物质 | ||
| 其他阳离子 | 氟硅酸 氟硅酸钠 | |
| 相关化学品 | 氟硼酸钾 | |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | ||
天然存在
编辑氟硅酸钾以Hieratit 和Demartinit 的形式天然存在。[6]
性质
编辑白色无臭无味六方或立方结晶或粉末。相对密度3.08(六方)或2.665(立方,17°C)。有吸湿性。微溶于水,可溶于盐酸,溶解度随温度升高而略有增加。不溶于醇。在热水中水解[7]生成硅酸和氟化氢[2]。有毒!
氟硅酸钾是立方晶系的,空间群 Fm3m (No. 225)。第二种形态(空间群 P63mc (No. 186))也是已知的。[4][8]
制备
编辑用途
编辑用作防腐蚀材料,木材防腐剂,冶金中镁和铝冶炼的助剂,钾玻璃、光学玻璃和不透明玻璃的制造原料。[1]也用于制取杀虫剂、有机中间体、化学分析、陶瓷和合成云母等。
参考文献
编辑- ^ 1.0 1.1 1.2 44495 Potassium hexafluorosilicate, 99.999% (metals basis), www.alfa.com, [2021-05-31], (原始内容存档于2016-12-28)
- ^ 2.0 2.1 2.2 2.3 Record of Kaliumhexafluorosilikat in the GESTIS Substance Database from the IFA
- ^ Loehlin, J. H., Redetermination of the structure of potassium hexafluorosilicate, K2SiF6, Acta Crystallogr., 1984, C40 (3): 570, doi:10.1107/S0108270184004893
- ^ 4.0 4.1 R. Blachnik. Taschenbuch für Chemiker und Physiker Band 3: Elemente, anorganische Verbindungen und Materialien, Minerale. Springer-Verlag. 2013: 524. ISBN 978-3-642-58842-6.
- ^ Dale L. Perry. Handbook of Inorganic Compounds, Second Edition. CRC Press. 2016: 324. ISBN 978-1-4398-1462-8.
- ^ mineralienatlas.de: Mineralienatlas Lexikon - Hieratit (页面存档备份,存于互联网档案馆), abgerufen am 21. November 2016
- ^ D. Menz, W. Wilde, L. Kolditz, K. Heide: Dynamisch thermische analyse der Zersetzung von K2SiF6. In: Journal of Fluorine Chemistry. 24 (3), 1984, S. 345–354, doi:10.1016/S0022-1139(00)81323-8.
- ^ J. H. Loehlin. Redetermination of the structure of potassium hexafluorosilicate, K2SiF6. 1984-03-15: 570–570. doi:10.1107/s0108270184004893.
- ^ Jane E. Macintyre. Dictionary of Inorganic Compounds. CRC Press. 1992: 3217. ISBN 978-0-412-30120-9.