五氯化鉬
五氯化鉬是一種無機化合物,化學式為[MoCl5]2,是一個二聚體。這種暗色揮發性的固體可用於製備其它鉬化合物的研究。它對濕氣敏感,可溶於氯代溶劑。[1]
| 五氯化鉬 | |
|---|---|

| |
| |

| |
| IUPAC名 Molybdenum(V) chloride Molybdenum pentachloride | |
| 識別 | |
| CAS號 | 10241-05-1 |
| PubChem | 61497 |
| EINECS | 233-575-3 |
| RTECS | QA4690000 |
| 性質 | |
| 化學式 | Mo2Cl10 |
| 摩爾質量 | 273.227(單體) 546.454(二聚體) g·mol⁻¹ |
| 外觀 | 暗綠色潮解性固體 |
| 密度 | 2.928 g/cm3 |
| 熔點 | 194 °C(467 K) |
| 沸點 | 268 °C(541 K) |
| 溶解性(水) | 水解 |
| 溶解性 | 可溶於干乙醚和干乙醇 |
| 結構 | |
| 晶體結構 | 單斜晶系 |
| 配位幾何 | edge-shared bioctahedron |
| 危險性 | |
| 主要危害 | 氧化劑 水解釋放出氯化氫 |
| 閃點 | 不可燃 |
| 相關物質 | |
| 其他陰離子 | 五氟化鉬 |
| 其他陽離子 | 五氯化鎢 |
| 相關價態氯化物 | 二氯化鉬 三氯化鉬 四氯化鉬 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
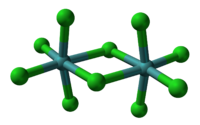
結構
編輯每個鉬具有local八面體對稱,在兩個鉬之間由兩個氯橋連接。[2]在W、Nb、Ta的五氯化物中,也發現了相似的結構。[3]在氣相中或溶液中的一部分,二聚體部分解離,得到單體五氯化物。[4]其單體具有順磁性,每個鉬中心具有一個未配對電子,形式氧化態為+5,在金屬中心留下一個價電子。
製備與性質
編輯MoCl5可以通過金屬鉬和氯氣反應得到,或由三氧化鉬的氯化得到。而MoCl6不穩定。[5]
MoCl5是一種強氧化劑,可以被乙腈還原,得到橙色配合物MoCl4(MeCN)2,它可以和THF反應,得到MoCl4(THF)2——其它含鉬配合物的前體。[6]MoCl5可以被HBr還原,生成四溴化鉬。在溴乙烷中(−50 °C)進行溴化反應,可以得到中間體MoBr5,它在20 °C分解,生成MoBr4和Br2:
- 2 MoCl5 + 10 HBr → 2 MoBr4 + 10 HCl + Br2
MoBr4和THF反應,生成含Mo(III)的物種mer-MoBr3(THF)3。[7]
MoCl5對於難被氧化的配體來說是一種優良的路易斯酸。它能和Cl−形成[MoCl6]−配離子。在有機合成中,該化合物偶爾會用於氯化反應、去氧反應和氧化偶聯反應。[8]
安全性
編輯MoCl5是一種強氧化劑,並且可以迅速水解,放出HCl。
參考文獻
編輯- ^ Holleman, A. F.; Wiberg, E. Inorganic Chemistry. San Diego, CA: Academic Press. 2001. ISBN 0-12-352651-5.
- ^ Beck, J.; Wolf, F. Three New Polymorphic Forms of Molybdenum Pentachloride. Acta Crystallogr. 1997, B53: 895–903. doi:10.1107/S0108768197008331.
- ^ Wells, A. E. Structural Inorganic Chemistry 5th. Oxford: Clarendon Press. 1984.
- ^ Brunvoll, J.; Ischenko, A. A.; Spiridonov, V. P.; Strand, T. G. Composition and Molecular Structure of Gaseous Molybdenum Pentachloride by Electron Diffraction. Acta Chem. Scand. 1984, A38: 115–120. doi:10.3891/acta.chem.scand.38a-0115.
- ^ Tamadon, Farhad; Seppelt, Konrad. The Elusive Halides VCl5, MoCl6, and ReCl6. Angew. Chem. Int. Ed. 2013, 52: 767–769. doi:10.1002/anie.201207552.
- ^ Dilworth, J. R.; Richards, R. L. The Synthesis of Molybdenum and Tungsten Dinitrogen Compounds. Inorg. Synth. 1990, 28: 33–45. ISBN 0-471-52619-3.
- ^ Calderazzo, F.; Maichle-Mössmer, C.; Pampaloni, G.; Strähle, J. Low-temperature Syntheses of Vanadium(III) and Molybdenum(IV) Bromides by Halide Exchange. Dalton Trans. 1993, 1993: 655–658. doi:10.1039/DT9930000655.
- ^ Kauffmann, T.; Torii, S.; Inokuchi, T. Molybdenum(V) Chloride. Encyclopedia of Reagents for Organic Synthesis. New York, NY: J. Wiley & Sons. 2004. doi:10.1002/047084289.