氯丁二烯
氯丁二烯,即2-氯-1,3-丁二烯,化学式为CH2=CCl-CH=CH2。它在室温下是无色液体,主要用作生产氯丁橡胶的单体。
| 氯丁二烯 | |||
|---|---|---|---|
| |||
| IUPAC名 2-Chloro-1,3-butadiene | |||
| 别名 | 2-氯-1,3-丁二烯 | ||
| 识别 | |||
| CAS号 | 126-99-8 | ||
| PubChem | 31369 | ||
| ChemSpider | 29102 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | YACLQRRMGMJLJV-UHFFFAOYAQ | ||
| ChEBI | 39481 | ||
| RTECS | EL9625000 | ||
| KEGG | C19208 | ||
| 性质 | |||
| 化学式 | C4H5Cl | ||
| 摩尔质量 | 88.5365 g·mol⁻¹ | ||
| 外观 | 无色液体 | ||
| 密度 | 0.9598 g/cm3 (液) | ||
| 熔点 | -130 °C(143 K) | ||
| 沸点 | 59.4 °C(333 K) | ||
| 溶解性(水) | 0.026 g/100 mL (液) | ||
| 危险性 | |||
| 警示术语 | R:R45, R11, R20/22, R36/37/38, R48/20 | ||
| 安全术语 | S:S53, S45 | ||
| 主要危害 | 高度可燃、有毒 | ||
| NFPA 704 | |||
| 闪点 | -15.6°C | ||
| 相关物质 | |||
| 相关二烯烃 | 丁二烯、异戊二烯 | ||
| 相关化学品 | 氯乙烯 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
氯丁二烯的工业生产以丁二烯为原料,涉及三步:
- 氯化,氯气与丁二烯发生加成反应,生成3,4-二氯-1-丁烯和2,3-二氯-2-丁烯的混合物;
- 异构化,2,3-二氯-2-丁烯转化为3,4-二氯-1-丁烯;
- 脱卤化氢,用碱处理生成2-氯-1,3-丁二烯。
1983年用此法制得的氯丁二烯大约为两百万吨,[1]杂质主要是1-氯-1,3-丁二烯,可通过蒸馏除去。
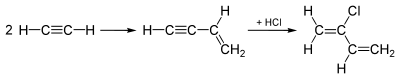
1960年以前的制取方法以乙炔为原料。先由乙炔二聚得到乙烯基乙炔,与氯化氢加成得到4-氯-1,2-丁二烯,在氯化亚铜存在下重排,生成氯丁二烯。[2][1]
该法能源的消耗量较大,投资费用较高,并且中间体乙烯基乙炔也是不稳定的。
参考资料
编辑- ^ 1.0 1.1 Manfred Rossberg, Wilhelm Lendle, Gerhard Pfleiderer, Adolf Tögel, Eberhard-Ludwig Dreher, Ernst Langer, Heinz Rassaerts, Peter Kleinschmidt, Heinz Strack, Richard Cook, Uwe Beck, Karl-August Lipper, Theodore R. Torkelson, Eckhard Löser, Klaus K. Beutel, "Chlorinated Hydrocarbons" in Ullmann's Encyclopedia of Industrial Chemistry, 2006 John Wiley-VCH: Weinheimdoi:10.1002/14356007.a06_233.pub2
- ^ Wallace H. Carothers, Ira Williams, Arnold M. Collins, and James E. Kirby. Acetylene Polymers and their Derivatives. II. A New Synthetic Rubber: Chloroprene and its Polymers. J. Am. Chem. Soc. 1937, 53: 4203–4225. doi:10.1021/ja01362a042.