配位域
在配位化學中 ,第一配位域是指直接與中心金屬原子相連的分子和離子( 配體 )。 第二配位域指以各種方式連接到第一配位域的分子和離子。
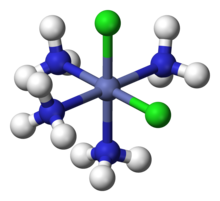
2(NH
3)
4]+
分子,其中NH
3和Cl基團圍繞中心鈷離子形成配位域。
第一配位域 編輯
第一配位域指直接附着在金屬上的那些分子。 第一和第二配位域之間的相互作用通常涉及氫鍵。 對於帶電配合物來說, 離子的相互作用很重要。
離子的第一配位域。
在三氯化六氨合鈷(III) [Co(NH
3)
6]Cl
3中,鈷離子和6個氨配體組成第一配位域。 這個離子的配位球由中央MN6核心組成,它向外輻射出18條N-H鍵。
第二配位域 編輯
4·7H
2O中,Fe2+
的第一配位域由六個水配體組成,而第二配位域由結晶水和硫酸鹽組成 ,它們與[Fe(H
2O)
6]2+
中心相互作用。
金屬離子可以描述為由兩個同心的配位域組成,也就是第一配位域和第二配位域。 溶劑分子表現得更像本體溶劑,因為它離第二配位域更遠。 對於第二配位域的模擬是計算化學的熱點。第二配位域可以由離子(尤其是在帶電絡合物中),分子(尤其是氫與第一配位域中的配體連接的分子)或部分的配體主鏈組成。 與第一配位域相比,第二配位域對金屬絡合物的反應活性和化學性質的影響較小。 然而,第二配位領域仍然與理解金屬絡合物的反應有關,比如配體交換和催化的機理。
在催化中的作用 編輯
金屬蛋白的機制通常會調用該蛋白對第二配位域進行調節。例如,某些氫化酶的第二配位域中的胺輔因子有助於活化二氫底物。[1]
在機械無機化學中的作用 編輯
第一配體和第二配體之間配體交換的速率是配體取代反應的第一步。 在締合配體取代中 ,親核試劑進入的是第二配位域。 這些影響與MRI中使用的造影劑這類實際應用有關。[4]
內域電子轉移反應的能量通過第二配位域來討論。 一些質子耦合電子轉移反應涉及反應物第二配位域之間的原子轉移:
[Fe(H
2O)
6]2+
+ [Fe(H
2O)
5(OH)]2+
→ [Fe(H
2O)
6]3+
+ [Fe(H
2O)
5(OH)]2+
在光譜學中的作用 編輯
溶劑對顏色和穩定性的影響通常是因為第二配位域的變化。 在第一配位域中的配體是強氫鍵供體和受體,例如在[Co(NH
3)
6]3+
和[Fe(CN)
6]3−
配合物中,這種作用會非常明顯。 冠醚通過其第二配位域與多胺絡合物結合。 聚銨陽離子與氰基金屬鹽的氮中心相結合。 [5]
在超分子化學中的作用 編輯
參見 編輯
參考文獻 編輯
- ^ J. C. Fontecilla-Camps, A. Volbeda, C. Cavazza, Y. Nicolet "Structure/Function Relationships of [NiFe]- and [FeFe]-Hydrogenases" Chem. Rev. 2007, 107, 4273-4303. doi:10.1021/cr050195z
- ^ Yang, J. Y.; Chen, S.; Dougherty, W. G.; Kassel, W. S.; Bullock, R. M.; DuBois, D. L.; Raugei, S.; Rousseau, R.; Dupuis, M. Hydrogen oxidation catalysis by a nickel diphosphine complex with pendant tert-butyl amines. Chem. Commun. 2010, 46 (45): 8618–8620. PMID 20938535. doi:10.1039/c0cc03246h.
- ^ Bullock, R. M.; Helm, M. L. Molecular Electrocatalysts for Oxidation of Hydrogen Using Earth-Abundant Metals: Shoving Protons Around with Proton Relays. Acc. Chem. Res. 2015, 48 (7): 2017–2026 [2020-07-27]. OSTI 1582563. PMID 26079983. doi:10.1021/acs.accounts.5b00069. (原始內容存檔於2020-07-27).
- ^ R. M. Supkowski, W. DeW.
- ^ Lehn, J. M. Supramolecular Chemistry: Concepts and Perspectives; VCH: Weinhiem, 1995.
- ^ Z. Liu, S. T. Schneebeli, J. F. Stoddart "Second-sphere coordination revisited" Chimia 2014, 68, 315-320. doi:10.2533/chimia.2014.315
- ^ Z. Liu, M. Frasconi, J. Lei, Z. J. Brown, Z. Zhu, D. Cao, J. Iehl, G. Liu, A. C. Fahrenbach, O. K. Farha, J. T. Hupp, C. A. Mirkin, Y. Y. Botros, J. F. Stoddart "Selective isolation of gold facilitated by second-sphere coordination with alpha-cyclodextrin" Nature Communications 2013, 4, 1855. doi:10.1038/ncomms2891