硫酸铍
化合物
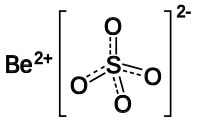
硫酸铍是一种无机化合物,化学式为BeSO4,它通常以四水合物[Be(H2O)4]SO4的形式存在,为无色晶体。硫酸铍最早于1815年被永斯·贝采利乌斯发现。[3] 硫酸铍易溶于水,微溶于浓硫酸。[4]
| 硫酸铍 | |
|---|---|
| |

| |
| 识别 | |
| CAS号 | 13510-49-1(无水) 7787-56-6(四水) |
| PubChem | 26077 |
| ChemSpider | 24291 |
| SMILES |
|
| InChI |
|
| InChIKey | KQHXBDOEECKORE-NUQVWONBAA |
| EINECS | 236-842-2 |
| ChEBI | 53473 |
| RTECS | DS4800000 |
| 性质 | |
| 化学式 | BeSO4 |
| 摩尔质量 | 105.075 g/mol(无水) 177.136 g/mol(四水) g·mol⁻¹ |
| 外观 | 白色固体或无色晶体 |
| 氣味 | 无味 |
| 密度 | 2.44 g/cm3(无水) 1.71 g/cm3(四水) |
| 熔点 | 110 °C(383 K)(四水合物,−2H2O) 400 °C(673 K)(二水,完全失水) 550—600 °C(823—873 K)(分解) |
| 沸点 | 2,500 °C(2,770 K)(无水) 580 °C(853 K)(四水) |
| 溶解性(水) | 36.2 g/100 mL (0 °C) 40.0 g/100 mL (20 °C) 54.3 g/100 mL (60 °C) |
| 溶解性 | 难溶于乙醇 |
| 折光度n D |
1.4374(四水) |
| 热力学 | |
| ΔfHm⦵298K | -1197 kJ/mol |
| S⦵298K | 90 J/mol K |
| 危险性 | |
GHS危险性符号  
| |
| GHS提示词 | 危险 |
| H-术语 | H350, H330, H301, H372, H319, H335, H315, H317, H411 |
| 闪点 | 不可燃 |
| PEL | TWA 0.002 mg/m3 C 0.005 mg/m3 (30分钟), 峰值为0.025 mg/m3 (以Be计)[1] |
| 致死量或浓度: | |
LD50(中位剂量)
|
82 mg/kg (大鼠,经口) 80 mg/kg (小鼠,经口)[2] |
| 相关物质 | |
| 其他阳离子 | 硫酸镁 硫酸钙 硫酸鍶 硫酸钡 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备及结构
编辑硫酸铍可以由其它铍化合物和硫酸反应,蒸发溶液后结晶得到。水合物在400 °C加热得到无水物。[5]四水合物有四面体的Be(OH2)42+单元和硫酸根离子。Be2+阳离子的半径小,使配位水分子的数量比同族MgSO4·6H2O中的Mg(OH2)62+配离子的配位水数目少。[6]
无水物的结构和块磷铝矿的结构类似,结构中四面体配位的Be和S原子交替排布,每个氧为二配位(Be-O-S)。分子中Be-O的键长为156 pm;S-O的键长为150 pm。[7]
性质及用途
编辑- BeSO4 → BeO + SO3
参考文献
编辑- ^ NIOSH Pocket Guide to Chemical Hazards. #0054. NIOSH.
- ^ "NIOSH Pocket Guide to Chemical Hazards #0054". National Institute for Occupational Safety and Health (NIOSH).
- ^ Lathrop Parsons, Charles, The Chemistry and Literature of Beryllium, London: 29–33, 1909.
- ^ 张维杰, 张钦良, 李又明. 剧毒物品实用技术手册. 北京: 人民交通出版社, 1996. ISBN 7-114-03020-7.
- ^ Patnaik, Pradyot, Handbook of Inorganic Chemicals, McGraw-Hill, 2002, ISBN 0-07-049439-8.
- ^ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
- ^ Grund, Alfred. Die Kristallstruktur von BeSO4. Tschermaks Mineralogische und Petrographische Mitteilungen. 1955, 5 (3): 227–230. ISSN 0041-3763. doi:10.1007/BF01191066.
- ^ 王小锋, 王日初, 彭超群,等. 聚丙烯酰胺凝胶法制备纳米BeO粉体前驱体的热分解过程及结晶机理[J]. 中国有色金属学报, 2012(8):2295-2301.
- ^ 无机化学丛书 第二卷 铍 碱土金属 硼 铝 镓分族. 科学出版社. pp 52-54
- ^ 赵晓萌. 金属(亚)磷酸盐、有机膦酸盐的水热合成及性能研究[D]. 青岛大学, 2016.
- ^ Radium - chemical element. Encyclopedia Britannica. [2018-07-10]. (原始内容存档于2018-07-10).
拓展链接
编辑- 国际化学品安全卡1351
- IARC Monograph "Beryllium and Beryllium Compounds"
- IPCS Health & Safety Guide 44 (页面存档备份,存于互联网档案馆)
- IPCS CICAD 32 (页面存档备份,存于互联网档案馆)
- 胡子南, 龙圣喜, 肖功华,等. 铍的急性、慢性、蓄积性和诱变性研究 (页面存档备份,存于互联网档案馆)[J]. 毒理学杂志, 1990(2):123-123.