臭氧
| 此條目需要补充更多来源。 (2014年7月23日) |
臭氧(英語:ozone)即三氧(trioxygen,化学式:O3),是氧的单质三原子分子,是氧气(双氧)的同素异形体,在常温下是一种有刺鼻味道的淡蓝色气体。臭氧的英语称呼源自希腊语的中性现在时分词 ozein (ὄζειν),意为“嗅”。
| 臭氧 | |||
|---|---|---|---|
| |||
| |||

| |||
| IUPAC名 Trioxygen | |||
| 英文名 | Ozone | ||
| 识别 | |||
| CAS号 | 10028-15-6 | ||
| PubChem | 24823 | ||
| ChemSpider | 23208 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | CBENFWSGALASAD-UHFFFAOYAY | ||
| Gmelin | 1101 | ||
| EINECS | 233-069-2 | ||
| ChEBI | 25812 | ||
| RTECS | RS8225000 | ||
| MeSH | Ozone | ||
| 性质 | |||
| 化学式 | O3 | ||
| 摩尔质量 | 47.998 [1] g·mol⁻¹ | ||
| 外观 | 浅蓝色气体[1] | ||
| 密度 | 0.002144 g/cm3 (0 ℃) 0.001962g/cm3(25 ℃)[1] | ||
| 熔点 | -193 ℃[1] | ||
| 沸点 | -111.35 ℃[1] | ||
| 溶解性(水) | 1.05 g/dm3 (0 °C) | ||
| 折光度n D |
1.2226(液態) | ||
| 结构 | |||
| 空间群 | C2v | ||
| 配位几何 | 對角線 | ||
| 分子构型 | 二面角 | ||
| 混成軌域 | sp2 for O1 | ||
| 偶极矩 | 0.53 D | ||
| 热力学 | |||
| ΔfHm⦵298K | 142.67 kJ·mol−1 | ||
| S⦵298K | 238.92 J·mol-1·K-1 | ||
| 危险性 | |||
| 欧盟分类 | |||
| NFPA 704 | |||
| 相关物质 | |||
| 相关化学品 | 二氧化硫 三硫 一氧化二硫 环臭氧 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
臭氧主要存在于距地球表面20公里的平流层下部的臭氧层中,含量約50ppm,主要由日光中的紫外线照射双氧产生光解而成,少量由大气层中的放电现象(闪电)电解产生。臭氧是一种比氧气更活跃的氧化剂,能吸收对生物细胞和遗传物质有害的短波紫外线,防止其到达地表。
發現 编辑
1785年,德国人馬丁·范·馬倫在做實驗時,發現發電機附近有股異味,但是他並沒有繼續研究下去。[2]1839年,另一德裔瑞士化學家克里斯提安·弗里德里希·尚班在做電解水實驗亦發現特殊的臭味,[3]於是他以「ozone」來命名這種新氣體,來源自希臘語「ozein」,意思是「臭味」,並於1840年在《哲學雜誌》上發表相關他的發現。[4]
物理性質 编辑
臭氧是一種淡藍色氣體,微溶於水,易溶於四氯化碳或碳氟化合物而顯藍色。在-112℃凝結成深藍色的液體。溫度低於-193℃,臭氧會形成紫黑色固體。
大多數人都可以嗅到有點類似氯刺鼻的氣味。暴露在0.1-1 ppm的臭氧會產生頭痛,眼睛灼熱,刺激呼吸道。即使空氣中有低濃度的臭氧,也會破壞有機材料,如橡膠、塑料,及動物的肺部組織。
性狀 编辑
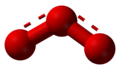
臭氧具有等腰三角形結構,含有一个3中心4电子离域π键,三個氧原子分別位於三角形的三個頂點,頂角為116.79度,密度约為氧氣的1.5倍,其沸點和凝固點均高於氧。臭氧在液態時呈現藍紫色,在固態呈現紫色。[5]它與氧氣不同,高濃度的臭氧帶明顯令人噁心的氣味。但低浓度的臭氧闻起来就像下过雨后出门闻到的“新鲜空气”的那种气味,十分怡人。臭氧反應活性強,極易分解,很不穩定,在常溫下會逐漸分解為氧氣。臭氧性質比氧活潑,比重為一般空氣的1.7倍。臭氧會因光、熱、水份、金屬、金屬氧化物以及其他的觸媒而加速分解為氧。
它不溶於液態氧等。有很強的氧化性,在常溫下可將銀氧化成氧化銀,將硫化鉛氧化成硫酸鉛。臭氧可使許多有機色素褪色,對橡膠和纖維破壞性很大,很容易氧化有機不飽和化合物。臭氧在冰中極為穩定,其半衰期為2000年。
臭氧可利用碘化鉀來檢驗。
臭氧能迅速且定量地氧化I−
成I
2,此反应也可以用来测定O
3的含量。[6]
臭氧能氧化CN−
故常被用来处理电镀工业中的含氰废水[6] :
由于它的强氧化性,亦可用于消毒杀菌剂。[6]
結構 编辑
臭氧分子呈弯曲形对称结构。中心原子采取sp²杂化(混成),两个杂化轨道与其他两个氧原子形成两根σ键,另一杂化轨道容纳孤对电子,除此之外,互相平行的2pz轨道重叠形成三中心四电子的大π键。
臭氧分子可以结合一个电子形成臭氧根离子(O3-),所形成的化合物为离子型臭氧化合物。臭氧分子也可以形成臭氧链-O-O-O-,构成共价型臭氧化物,如O3F2。[7]
臭氧层 编辑
在大氣層中,氧分子因高能量的輻射而分解為氧原子(O),而氧原子與另一氧分子結合,即生成臭氧。臭氧又會與氧原子、氯或其他游離性物質反應而分解消失,由於這種反覆不斷的生成和消失,乃能使臭氧含量維持在一定的均衡狀態,而大氣中約有90%的臭氧存在於離地面15到50公里之間的區域,也就是平流層,在平流層的較低層,即離地面20到30公里處,為臭氧濃度最高之區域,是為臭氧層(ozone layer)。
用途與制備 编辑
工业上,用干燥的空气或氧气,采用5-25kv的交流电压进行无声放电制取,用空气做氧源时会衍生出大量氮氧化合气体。目前最先进的臭氧制备方法为高能量紫外线光解空气而对应生成纯净的臭氧。另外,在低温下电解稀硫酸,或将液体氧气加热都可制得臭氧。大自然很容易產生臭氧,在打雷閃電時會產生幾十萬伏特的高壓電,電離空氣及有機物形成臭氧。臭氧能於短時間內將空氣中的浮游細菌消滅,並能中和、分解毒氣,去除惡臭。臭氧作为一种常温下的气态强氧化剂,能迅速弥漫到整个灭菌空间,灭菌不留死角,杀菌更彻底。因此臭氧可用于净化空气及饮用水、杀菌、处理工业废物和作为漂白剂。在一些游泳池以臭氧取代氯气做為消毒用途。
市面上有一部分的空氣清淨機(或活氧機)具有製造活氧的功能,其實活氧就是臭氧,因為臭氧對生物有危害,在使用時人跟寵物都不能在室內。
三聚體的三過氧化三丙酮分解也可以產生臭氧,但反應較為劇烈,不宜使用:
臭氧的灭菌原理:灭菌过程属生物化学氧化反应。臭氧能对细菌的细胞体直接氧化,即破坏其DNA而达到抑制的效果,对病毒的RNA亦有破坏作用;对各种毒素具有一定的氧化作用,降低其毒性。
- 臭氧能氧化分解细菌内部葡萄糖所需的酶,使细菌灭活死亡。
- 直接与细菌、病毒作用,破坏它们的细胞器和DNA、RNA,使细菌的新陈代谢受到破坏,导致细菌死亡。
- 透过细胞膜组织,侵入细胞内,作用于外膜的脂蛋白和内部的脂多糖,使细菌发生通透性畸变而溶解死亡。
臭氧對人體的影響 编辑
臭氧具有強烈的刺激性,吸入過量對人體健康有一定危害。它主要是刺激和損害深部呼吸道,並可損害中樞神經系統,對眼睛有輕度的刺激作用。
臭氧吸入体内后,能迅速转化为活性很强的自由基-超氧基(O₂⁻),主要使不饱和脂肪酸氧化,从而造成细胞损伤。[8]
當大氣中臭氧濃度為0.1mg/m3時,可引起鼻和喉頭粘膜的刺激;臭氧濃度在0.1-0.2mg/m3時,引起哮喘發作,導致上呼吸道疾病惡化,同時刺激眼睛,使視覺敏感度和視力降低[來源請求]。臭氧濃度在2mg/m3以上可引起頭痛、胸痛、思維能力下降,嚴重時可導致肺氣腫和肺水腫。
此外,臭氧還會阻礙血液輸氧功能,造成組織缺氧;使甲狀腺功能受損、骨骼鈣化,還可引起潛在性的全身影響,如誘發淋巴細胞染色體畸變,損害某些酶的活性和產生溶血反應。臭氧超過一定濃度,除對人體有一定毒害外,對某些植物生長也有一定危害。臭氧還可以使橡膠製品變脆和產生裂紋。臭氧對人體也有致畸性,母亲孕期接触臭氧可导致新生儿睑裂狭小发生率增多。[9]
参见 编辑
參考文獻 编辑
- ^ 1.0 1.1 1.2 1.3 1.4 CRC Handbook of Chemistry and Physics 97th Edition. 2016-06-24: 4–77. ISBN 1-4987-5428-7 (英语).
- ^ 陳興漢; 廖品姍. 生物氧化醫學問與答. 台北: 漢珍. 2018-07-10. ISBN 9789869613583.
- ^ Schönbein, C. F. Lecture of 13 March 1839. Ber. Verh. Nat. Ges. Basel. 1838–1840, 4: 58.
- ^ Schönbein, C. F. On the Odour Accompanying Electricity and on the Probability of its Dependence on the Presence of a New Substance. Philosophical Magazine. 1840, 17: 293–294.
- ^ ChemicalForce. That's how liquid ozone explodes!. [2021-07-19]. (原始内容存档于2022-01-27).
- ^ 6.0 6.1 6.2 武汉大学 吉林大学等校编 曹锡章 宋天佑 王杏乔修订. 无机化学(第三版). 高等教育出版社. 1994-10: 573 [2017-10-22]. ISBN 978-7-04-004880-3 (中文).
- ^ 刘新锦等.无机元素化学 氧族元素.北京:科学出版社.2010.01 ISBN 978-7-03-026399-5
- ^ 王旭梅; 柳若安; 曹磊; 冯晶; 李燚佩; 孙建强. 《环境标志产品技术要求 食具消毒柜 (征求意见稿)》 编制说明 (PDF). 环境保护部环境发展中心(中日友好环境保护中心). 2017年9月 [2020-07-16]. (原始内容存档 (PDF)于2020-07-16).
- ^ 《常见有毒化学品应急救援手册》,中山大学出版社


