辅酶Q–细胞色素c还原酶
辅酶Q: 细胞色素c - 还原酶(英語:coenzyme Q : cytochrome c – oxidoreductase,),有时被称为细胞色素bc1复合体,又有时被称为复合体III(第三复合体,complex III),是電子傳遞鏈的第三个复合体(EC 1.10.2.2),在生化生成ATP(氧化磷酸化)中发挥关键作用。 复合体III是由线粒体(细胞色素b)和核心基因组(所有其他亚基)编码的多亚基跨膜蛋白。 复合体III存在于所有动物的线粒体和所有需氧真核生物和大多数细菌的内膜中。 复合体III中的突变导致运动不耐受以及多系统疾病。 bc1复合体含有11个亚基,3个呼吸亚单位(细胞色素B,细胞色素C1,Rieske蛋白),2个核心蛋白,和6个低分子量蛋白。
| UCR_TM | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| 鑑定 | |||||||||
| 標誌 | UCR_TM | ||||||||
| Pfam | PF02921(旧版) | ||||||||
| InterPro | IPR004192 | ||||||||
| SCOP | 1be3 / SUPFAM | ||||||||
| TCDB | 3.D.3 | ||||||||
| OPM家族 | 92 | ||||||||
| OPM蛋白 | 3cx5 | ||||||||
| 膜蛋白數據庫 | 258 | ||||||||
| |||||||||
| ubiquinol—cytochrome-c reductase | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
| 识别码 | |||||||
| EC編號 | 7.1.1.8 | ||||||
| CAS号 | 9027-03-6 | ||||||
| 数据库 | |||||||
| IntEnz | IntEnz浏览 | ||||||
| BRENDA | BRENDA入口 | ||||||
| ExPASy | NiceZyme浏览 | ||||||
| KEGG | KEGG入口 | ||||||
| MetaCyc | 代谢路径 | ||||||
| PRIAM | 概述 | ||||||
| PDB | RCSB PDB PDBj PDBe PDBsum | ||||||
| 基因本体 | AmiGO / EGO | ||||||
| |||||||
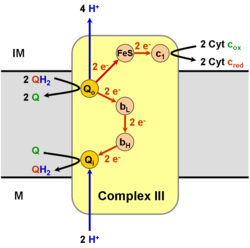
- QH2 + 2 高铁细胞色素c Q + 2 亚铁细胞色素c + 2 H+
因此,此酶的两个底物分别是二氢醌(QH2)与高铁(Fe3+)细胞色素c,而其三个产物则分别是醌(Q)、亚铁(Fe2+)细胞色素c以及H+。
该酶属于氧化还原酶家族,特别是那些作用于细胞色素作为受体的作为供体的二酚和相关物质的氧化还原酶。 该酶参与氧化磷酸化。 它有四种辅助因子:细胞色素c1,细胞色素b-562,细胞色素b-566,和Rieske型的2-铁铁氧还蛋白。
命名法 编辑
该酶类的系统名称是泛醇:铁细胞色素-c 氧化还原酶(英語:ubiquinol:ferricytochrome-c oxidoreductase)。 其他常用名称包括:
|
|
结构 编辑
与電子傳遞鏈的其他主要质子泵亚基相比,发现的亚基数可以很小,小到三条多肽链。 这个数字增加了,在高等动物身上发现了11个亚基[2]。三个亚基有辅因子。 细胞色素b亚基具有两个b型血基質(bL和bH 英語:heme),Cytochrome C亚基具有一个c型血基質(c1),并且Rieske铁硫蛋白亚基(ISP)具有两个铁,两个硫的铁-硫簇(2Fe•2S)。
复合体的组成 编辑
在脊椎动物中,bc1复合体,或复合体III,含有11个亚基:3个呼吸亚基,2个核心蛋白,和6个低分子量蛋白[3][4]。 变形杆菌复合体可能含有少至三个亚基[5]。
复合体III的亚基组成表 编辑
| No. | 亚基名称 | 人类 蛋白质 | 来自UniProt的蛋白质描述 | 带有人类蛋白质的Pfam家族 |
|---|---|---|---|---|
| 呼吸亚基蛋白 | ||||
| 1 | MT-CYB / Cyt b | CYB_HUMAN | 细胞色素 b | Pfam PF13631 |
| 2 | CYC1 / Cyt c1 | CY1_HUMAN | 细胞色素 c1, 血基質蛋白, 线粒体的 | Pfam PF02167 |
| 3 | Rieske / UCR1 | UCRI_HUMAN | 细胞色素 b-c1 复合体 亚基 Rieske, 线粒体的 EC 1.10.2.2 | Pfam PF02921 , Pfam PF00355 |
| 核心蛋白亚基 | ||||
| 4 | QCR1 / SU1 | QCR1_HUMAN | 细胞色素 b-c1 复合体 亚基 1, 线粒体的 | Pfam PF00675, Pfam PF05193 |
| 5 | QCR2 / SU2 | QCR2_HUMAN | 细胞色素 b-c1 复合体 亚基 2, 线粒体的 | Pfam PF00675, Pfam PF05193 |
| 低分子量蛋白质亚基 | ||||
| 6 | QCR6 / SU6 | QCR6_HUMAN | Cytochrome b-c1 complex subunit 6, mitochondrial | Pfam PF02320 |
| 7 | QCR7 / SU7 | QCR7_HUMAN | Cytochrome b-c1 complex subunit 7 | Pfam PF02271 |
| 8 | QCR8 / SU8 | QCR8_HUMAN | Cytochrome b-c1 complex subunit 8 | Pfam PF02939 |
| 9 | QCR9 / SU9 / UCRC | QCR9_HUMANa | Cytochrome b-c1 complex subunit 9 | Pfam PF09165 |
| 10 | QCR10 / SU10 | QCR10_HUMAN | Cytochrome b-c1 complex subunit 10 | Pfam PF05365 |
| 11 | QCR11 / SU11 | QCR11_HUMAN | Cytochrome b-c1 complex subunit 11 | Pfam PF08997 |
- a 在脊椎动物中,来自Rieske蛋白的N-末端的8kDa的切割产物(信号肽)作为亚基9保留在复合体中。因此,亚基10和11对应于真菌QCR9p和QCR10p。
反应 编辑
它通过辅酶Q(CoQ),又称泛醌(Ubiquinone,UQ),的氧化催化细胞色素c的还原,同时从线粒体基质向膜间隙泵送4个质子:
- QH2 + 2 细胞色素 c (FeIII) + 2 H+
in → Q + 2 细胞色素 c (FeII) + 4 H+
out
在称为Q循环的过程中[6][7],从基质(M)消耗了2个质子,4个质子被释放到膜间空间(IM)中,2个电子被传递到细胞色素c。
反应机制 编辑
复合体III(细胞色素bc1,辅酶Q:细胞色素C氧化还原酶)的反应机制称为辅酶(“Q”)循环。 在这个循环中,四个质子被释放到正“P”侧(膜间空间),但只有两个质子从负“N”侧(基质)被吸收。 结果,在膜上形成质子梯度。 在整个反应中,两个泛醇被氧化成辅酶,一个辅酶被还原成泛醇。 在完整的机制中,两个电子通过两个细胞色素c中间体从泛醇转移到辅酶。
总体:
- 2 x QH2氧化成Q.
- 1 x Q还原到QH2
- 2 x Cyt c被还原
- 4 x H+ 被释放到膜间隙
- 从基质中拾取2 x H+
第1轮:
- 细胞色素b结合一个泛醇和一个泛醌。
- 2Fe / 2S中心和BL血红素各自从结合的泛醌中吸出电子,释放出两个氢进入膜间隙。
- 一个电子从2Fe / 2S中心转移到细胞色素c1,而另一个电子从BL血红素转移到BH血红素。
- 细胞色素c1将其电子转移到细胞色素c(不要与细胞色素c1混淆),BHHeme将其电子转移到附近的泛醌,导致形成ubisemiquinone。
- 细胞色素c扩散。第一个泛醇(现在被氧化成泛醌)被释放,而半醌仍然被束缚。
第2轮:
- 第二种泛醇与细胞色素b结合。
- 2Fe / 2S中心和BL血红素各自从结合的泛醌中吸出电子,释放出两个氢进入膜间隙。
- 一个电子从2Fe / 2S中心转移到细胞色素c1,而另一个电子从BL血红素转移到BH血红素。
- 细胞色素c1然后将其电子转移到细胞色素c,而附近的第1轮产生的半醌从BH血红素中获取第二个电子,以及来自基质的两个质子。
- 释放出第二种泛醇(现在被氧化成泛醌)以及新形成的泛醇[8]。
复合体III的抑制剂 编辑
有三组不同的复合体III抑制剂。
- 抗霉素A与Qi位点结合并抑制复合物III中的电子从血基质bH转移至氧化的Q(Qi位点抑制剂)。
- Myxothiazol和stigmatellin与Qo位点结合并抑制电子从还原的QH2转移到Rieske铁硫蛋白。 Myxothiazol和stigmatellin与Qo位点内不同但重叠的口袋结合。
- Myxothiazol更接近细胞色素bL(因此被称为“近端”抑制剂)。
- Stigmatellin远离血基质bL并且更接近Rieske铁硫蛋白,与之强烈相互作用。
一些已被商业化为杀真菌剂(甲氧基丙烯酸酯Strobilurin衍生物,其中最着名的是嘧菌酯Azoxystrobin; QoI抑制剂)和抗疟疾剂(atovaquone)。
参阅 编辑
参考文献 编辑
- ^ PDB 1ntz; Gao X, Wen X, Esser L, Quinn B, Yu L, Yu CA, Xia D. Structural basis for the quinone reduction in the bc1 complex: a comparative analysis of crystal structures of mitochondrial cytochrome bc1 with bound substrate and inhibitors at the Qi site. Biochemistry. August 2003, 42 (30): 9067–80. PMID 12885240. doi:10.1021/bi0341814.
- ^ Iwata S, Lee JW, Okada K, Lee JK, Iwata M, Rasmussen B, Link TA, Ramaswamy S, Jap BK. Complete structure of the 11-subunit bovine mitochondrial cytochrome bc1 complex. Science. July 1998, 281 (5373): 64–71. PMID 9651245. doi:10.1126/science.281.5373.64.
- ^ Zhang Z, Huang L, Shulmeister VM, Chi YI, Kim KK, Hung LW, et al. Electron transfer by domain movement in cytochrome bc1.. Nature. 1998, 392 (6677): 677–84. PMID 9565029. doi:10.1038/33612.
- ^ Hao GF, Wang F, Li H, Zhu XL, Yang WC, Huang LS, et al. Computational discovery of picomolar Q(o) site inhibitors of cytochrome bc1 complex.. J Am Chem Soc. 2012, 134 (27): 11168–76. PMID 22690928. doi:10.1021/ja3001908.
- ^ Yang XH, Trumpower BL. Purification of a three-subunit ubiquinol-cytochrome c oxidoreductase complex from Paracoccus denitrificans. J Biol Chem. 1986, 261 (26): 12282–9. PMID 3017970.
- ^ Kramer DM, Roberts AG, Muller F, Cape J, Bowman MK. Q-cycle bypass reactions at the Qo site of the cytochrome bc1 (and related) complexes. Methods in Enzymology 382. 2004: 21–45. ISBN 978-0-12-182786-1. PMID 15047094. doi:10.1016/S0076-6879(04)82002-0.
|journal=被忽略 (帮助) - ^ Crofts AR. The cytochrome bc1 complex: function in the context of structure. Annu. Rev. Physiol. 2004, 66: 689–733. PMID 14977419. doi:10.1146/annurev.physiol.66.032102.150251.
- ^ Ferguson SJ, Nicholls D, Ferguson S. Bioenergetics 3rd. San Diego: Academic. 2002: 114–117. ISBN 978-0-12-518121-1.
- ^ Holmes, J. H.; Sapeika, N; Zwarenstein, H. Inhibitory effect of anti-obesity drugs on NADH dehydrogenase of mouse heart homogenates. Research Communications in Chemical Pathology and Pharmacology. 1975, 11 (4): 645–6. PMID 241101.
深入阅读 编辑
- Marres CM, Slater EC. Polypeptide composition of purified QH2:cytochrome c oxidoreductase from beef-heart mitochondria. Biochim. Biophys. Acta. 1977, 462 (3): 531–548. PMID 597492. doi:10.1016/0005-2728(77)90099-8.
- Rieske JS. Composition, structure, and function of complex III of the respiratory chain. Biochim. Biophys. Acta. 1976, 456 (2): 195–247. PMID 788795.
- Wikstrom M, Krab K, Saraste M. Proton-translocating cytochrome complexes. Annu. Rev. Biochem. 1981, 50: 623–655. PMID 6267990. doi:10.1146/annurev.bi.50.070181.003203.
外部链接 编辑
- cytochrome bc1 complex site (Edward A. Berry) at lbl.gov
- cytochrome bc1 complex site (Antony R. Crofts) (页面存档备份,存于互联网档案馆) at uiuc.edu
- PROMISE Database: cytochrome bc1 complex at scripps.edu
- Interactive Molecular Model of Complex III (Requires MDL Chime)
- Template:UMichOPM - Calculated positions of bc1 and related complexes in membranes
- 醫學主題詞表(MeSH):Coenzyme+Q-Cytochrome-c+Reductase
